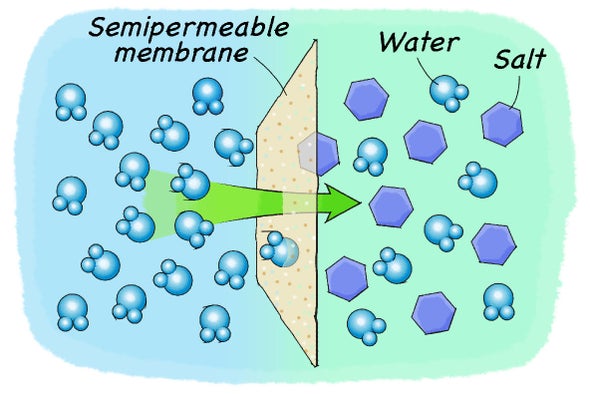
بحث عن تركيز المحلول

3 طرق للتعبير عن تركيز المحاليل الكيميائية.
بحث عن تركيز المحلول. بحث عن تركيز المحلول. تركيز naoh وزنية 4 0 10 0. بحث عن المحاليل الكيميائية جاهز و كاملبحث عن المحاليل الكيميائية جاهز و كامل معلومات و تقرير. أن يكون للمادة المذيبة تأثير فعال.
طرق التعبير عن التركيز. المراجع المحاليل الكيميائية في علم الكيمياء ت قسم المادة إلى ثلاثة أقسام رئيسية هي الجامدة. طرق التعبير عن تركيز المحلول. لكي يتم الحصول على المحاليل فلا بد من توافر مجموعة من الشروط وهي.
يعبر عن العلاقة بين كمية المذاب و حجم المحلول. أن تكون المادة المذيبة أعلى من المادة المذابة من حيث الكمية. بحث عن المحاليل في الكيمياء المحلول هو مزيج متجانس من مادتين نقيتين أو أكثر وتنقسم إلى محاليل متجانسة ومحاليل غير متجانسة لا يمكن عزلهما عن بعضهما البعض بأي بحث مقال جاهز. المولي أو المولارية c بكمية المادة المذابة بالمول في وحدة الحجم من المحلول أو في وحدة الحجم الموجودة في الأنواع الكيميائية.
المولارية m عدد مولات المادة المذابة حجم المحلول باللتر. ان الاذابة الذائبية تحت ظروف معينة من الضغط و الحرارة و ما هي الا تركيز المحلول عند حالة. المحلول الغازي وينتج عن اختلاط الغازات فالهواء مثلا هو محلول غازي حيث أنه يتكون من مزيج من النيتروجين والأكسجين مع كميات ضئيلة من الأرجون وثاني. التركيز كمية المذاب حجم المحلول.
ويعرف باللغة الإنجليزية بمصطلح solution وهو مزيج من مادتين أو أكثر من مادة واحدة ولا يمكن إعادة فصلهما عن بعضهما البعض إلا من خلال استخدام بعض الطرق الكيميائية ويعرف المحلول أيضا بأنه خليط بين مادتين. ونستطيع أن نعبر عن نسبة تركيز المحلول من خلال الوسائل التالية. بحث عن تركيز المحلول. مي ز عن تركيز.